IL-9靶向肺巨噬细胞介导肺中的过敏反应
作为肺中最丰富的免疫细胞之一,巨噬细胞是过敏反应的关键参与者。先前的研究表明,IL-9 (白细胞介素-9)会影响人类血液单核细胞和 AM 的氧化爆发,但对于 IL-9 如何影响肺巨噬细胞的异质性以及该功能如何与疾病发展相关联知之甚少。2022年2月,Science Immunology杂志上发表了一篇题为“An IL-9-pulmonary macrophage axis defines the allergic lung inflammatory environment”的文章,在这项研究中,研究者发现 IL-9 通过靶向肺巨噬细胞介导肺中的促过敏活动,揭示了IL-9/巨噬细胞/Arg1 轴作为过敏性气道炎症的潜在治疗靶点。
 研究者先是采用慢性HDM(house dust mite,房尘螨)感染模型,对WT(野生型)和Il9r-/-(IL-9受体敲除型)小鼠进行比较,Il9r-/-小鼠表现出比WT小鼠较轻的肺部炎症,表现为气道阻力、肺细胞浸润,总支气管肺泡灌洗液(BALF)细胞数、BALF嗜酸性粒细胞以及肺嗜酸性粒细胞数量,HDM特异性IgE水平及黏液量均显著降低。同时,IL-9R缺乏还会抑制肥大细胞的产生,但是T细胞、B细胞的数量或CD4+ T细胞产生的细胞因子IL9和IL13不受影响。通过骨髓(BM)嵌合体实验,发现WT→ Il9r-/-和Il9r-/-→WT嵌合体的整体炎症均降低,造血细胞中IL-9R缺失导致的炎症现象更明显,说明过敏反应期间造血细胞中IL-9/IL-9R信号传导的作用更强。(见图1)
研究者先是采用慢性HDM(house dust mite,房尘螨)感染模型,对WT(野生型)和Il9r-/-(IL-9受体敲除型)小鼠进行比较,Il9r-/-小鼠表现出比WT小鼠较轻的肺部炎症,表现为气道阻力、肺细胞浸润,总支气管肺泡灌洗液(BALF)细胞数、BALF嗜酸性粒细胞以及肺嗜酸性粒细胞数量,HDM特异性IgE水平及黏液量均显著降低。同时,IL-9R缺乏还会抑制肥大细胞的产生,但是T细胞、B细胞的数量或CD4+ T细胞产生的细胞因子IL9和IL13不受影响。通过骨髓(BM)嵌合体实验,发现WT→ Il9r-/-和Il9r-/-→WT嵌合体的整体炎症均降低,造血细胞中IL-9R缺失导致的炎症现象更明显,说明过敏反应期间造血细胞中IL-9/IL-9R信号传导的作用更强。(见图1)
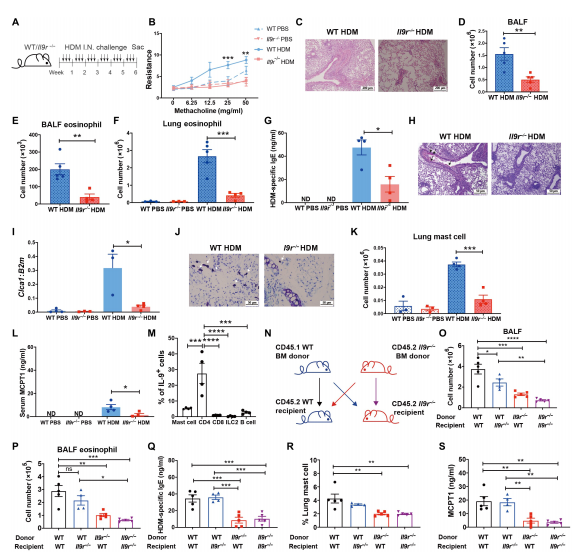
图1 缺乏IL-9R可抑制过敏性气道炎症
(图片来源于《Science Immunology》杂志)
通过流式细胞术,研究者发现在过敏性炎症的发展过程中,IL9或IL9R的缺失导致AM(alveolar macrophages,肺泡巨噬细胞)群体更好的维持以及CD11c-(整合素αX)和CD11c+ IM(interstitial macrophages,间质巨噬细胞)群体积累减少,Il9r-/- BM细胞成为 IM的倾向降低。还观察到在PBS处理组中肺细胞群种IL-9R+的细胞以肥大细胞、嗜碱性粒细胞、树突状细胞和AM为主;而HDM处理组则以巨噬细胞为主。研究者通过给小鼠鼻内注射IL-9,发现肺巨噬细胞减少和肥大细胞数量的增加。接着,为了验证 IL-9对肺巨噬细胞的特异性,研究者对WT小鼠注射IL-9或IL-13的阻断抗体,注射IL-9的小鼠气道阻力降低,AMs增加,IM抑制,抗IL-13抗体未能改变肺巨噬细胞群。(见图2)

图2 肺巨噬细胞是过敏性反应中关键的IL-9应答者
(图片来源于《Science Immunology》杂志)
通过对肺巨噬细胞和血液单核细胞进行CITE-seq(转录组和表位的细胞索引),得到6 个血单核细胞簇,14 个肺巨噬细胞簇。为了确定这些簇之间的关系,研究者使用CCR2+(趋化因子(C-C motif)受体2)作为根细胞类型进行伪时间分析,发现CD11c- IMs与血液单核细胞的关系最为密切,而AMs与CD11c- IMs或血液单核细胞的相似性最低。对从HDM处理小鼠中分离到的肺巨噬细胞通过细胞自旋分析形态,研究者发现AM和IM在其细胞质和细胞核中都显示出液泡,而AMs显示出更规则的圆形或椭圆形细胞核。通过转录组数据,研究者发现肺巨噬细胞群具有一些共同的转录谱,但它们的基因表达模式不同。此外,研究者还发现IL9R的缺失导致血液单核细胞和肺巨噬细胞群中基因表达的改变,IL-9信号显著促进巨噬细胞群中趋化因子的表达。这些数据说明肺巨噬细胞不仅充当IL-9应答者,而且可能参与IL-9 依赖性过敏反应。(见图3)
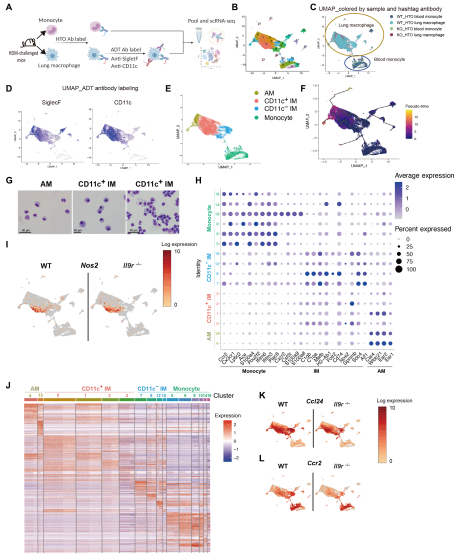
图3 过敏性炎症中肺巨噬细胞和血液单核细胞的异质性
(图片来源于《Science Immunology》杂志)
研究者通过鼻内或静脉注射氯膦酸钠,再利用流式细胞术发现小鼠气道的AMs细胞减少,CD11c的IMs细胞不受影响。静脉注射氯丙酸钠后小鼠气道的血液单核细胞和CD11c IMs减少,AM群体不受影响。在单核细胞和IMs数量减少后,WT小鼠的肺部炎症反应与Il9r -/-小鼠相似,说明血液单核细胞和IMs可能是过敏性气道炎症发生的必要条件。接着,研究者通过过继转移实验发现鼻内过继性移植WT CD11c- IMs或CD11c+ IMs增加了Il9r- /-小鼠的气道阻力和肺嗜酸性粒细胞的浸润。通过流式细胞术观察到,与WT小鼠相比,接受PBS处理的Il9r- /-小鼠显示出更小的MLN(纵隔淋巴结),CD11c- IMs或CD11c+ IMs的转移导致MLN的扩大,也就是说接受CD11c+ IMs的小鼠比WT小鼠有更大的淋巴结。说明肺巨噬细胞尤其是CD11c+ IMs和CD11c- IMs,参与了IL-9诱导的过敏性气道疾病。(见图4)
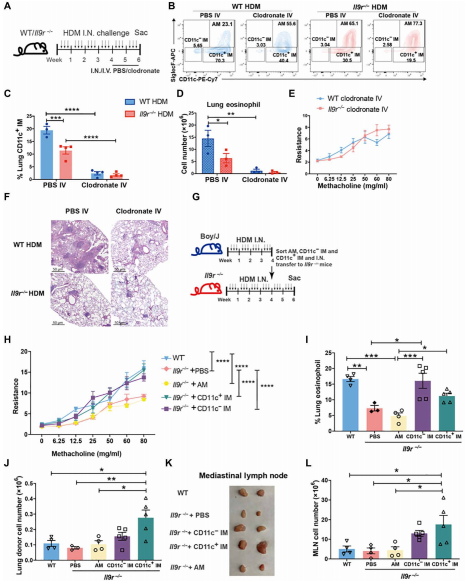
图4 肺巨噬细胞放大il -9介导的过敏性肺炎症
(图片来源于《Science Immunology》杂志)
研究者通过小鼠鼻内注射HDM发现,与野生型小鼠相比,HDM Il9r-/-小鼠的BM中保留了更多的单核细胞。然而,IL-9R表达与CCR2表达呈正相关,CCR2是单核细胞迁移所需的关键趋化因子受体,表明IL-9可能通过CCR2调节单核细胞向肺的迁移。随后在迁移实验中,研究者发现IL-9在CCL2存在时只促进单核细胞迁移。对HDM小鼠给予CCR2抑制剂后,与对照组小鼠相比,BM单核细胞增加,肺单核细胞、CD11c-和CD11c+ IM的细胞数显著减少,说明CD11c-和CD11c+ IM在肺中的积累依赖于CCR2+单核细胞。研究者将荧光珠标记的单核细胞转移到Il9r-/-小鼠中,流式细胞分析显示,IL-9信号通路促进单核细胞成为肺IMs。这些结果表明,在机制上IL-9抑制AMs的自我更新能力,促进单核细胞向肺募集,发展为IMs,IL-9信号通路可诱导单核细胞和IMs的促过敏功能。(见图5)
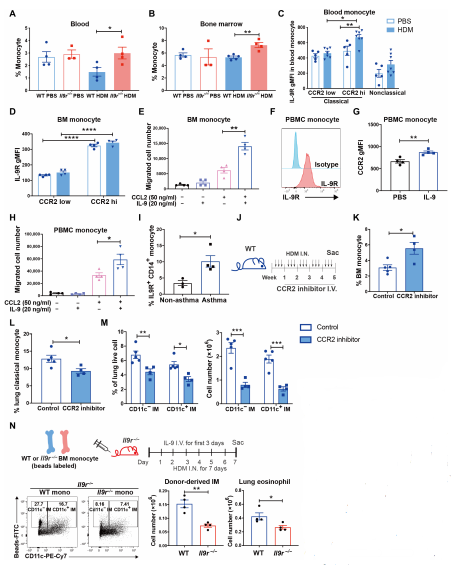
图5 IL-9通过招募单核细胞来增强过敏性炎症
(图片来源于《Science Immunology》杂志)
CITE-seq数据显示Il9r-/-小鼠Arg1(精氨酸酶)表达量降低,同样Il9r-/-小鼠肺IM群体中Arg1蛋白表达显著降低。研究者测定了HDM小鼠的血清中精氨酸酶活性,Arg1的表达量降低时,Il9r-/-小鼠的精氨酸酶活性明显低于WT小鼠。此外,在混合BM嵌合小鼠中,来自WT的Arg1+ IM细胞数量增加进一步证实了IL-9信号通路调节Arg1表达。研究者用IL-9对WT小鼠在体内、体外刺激后,发现IL-9促进了IMs中Arg1的表达。从HDM Il9r-/-且带有Arg1黄色荧光蛋白(YFP)报告基因(YARG)的小鼠中筛选出了表达和不表达Arg1的巨噬细胞,发现YFP+巨噬细胞迁移到肺中,并恢复了Il9r-/-小鼠肺中Arg1+巨噬细胞数量,YFP+ (Arg1+)巨噬细胞降低了Il9r-/-小鼠的过敏性肺炎症,而YFP-巨噬细胞则没有,说明Arg1+巨噬细胞参与IL-9介导的过敏反应。(见图6)
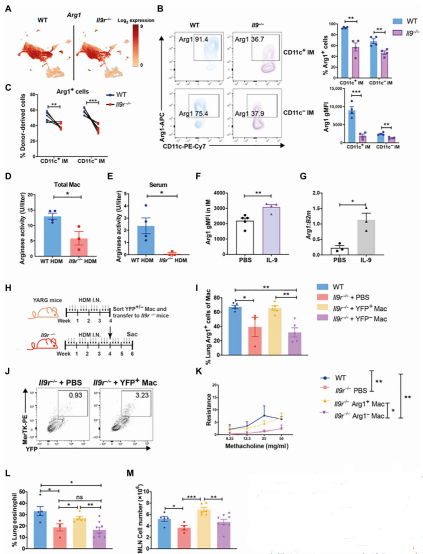
图6 IL-9通过调节Arg1表达影响肺巨噬细胞功能
(图片来源于《Science Immunology》杂志)
将Arg1fl/flLysM-Cre+或同窝对照组小鼠给予HDM刺激后,研究者发现IMs中Arg1表达降低,血清精氨酸酶活性降低,BALF总数量、BALF嗜酸性粒细胞、肺嗜酸性粒细胞和MLN细胞数量下降。在CITE-seq数据中,Il9r-/- IMs的Ccl5表达下降,缺乏Arg1的IMs也显示CCL5表达低于对照IMs。与ELISA检测的Arg1fl/flLysM-Cre+和Il9r-/-小鼠血清CCL5结果一致。在体外IL-9刺激下,Arg1+巨噬细胞比Arg-巨噬细胞分泌更多的CCL5;在体内,IL-9也增加了IMs中CCL5的表达。此外,研究者还发现来自HDM处理小鼠的Arg1+IMs比Arg1- IMs表达更多的CCL5。这些结果表明,IL-9调控过敏性气道炎症需要肺巨噬细胞中Arg1的表达,而Arg1+ IMs分泌更多的CCL5诱导嗜酸性粒细胞介导的过敏性炎症。
研究者分析了非哮喘和哮喘患者的IL-9浓度和精氨酸酶活性,与非哮喘患儿相比,哮喘儿童显示抗CD3刺激的PBMCs产生的IL-9增加,与肺功能呈负相关,并与血清精氨酸酶活性增加相关,哮喘患者也显示CCL5表达增加。IL-9的产生与血清CCL5水平呈正相关。这些数据表明IL-9通过增加肺巨噬细胞中Arg1和CCL5的表达来调节过敏性气道炎症。(见图7)

图7 IL-9通过诱导肺巨噬细胞产生CCL5来促进过敏性炎症
(图片来源于《Science Immunology》杂志)
总的来说,这些发现不仅对 IL-9 介导的过敏反应的理解具有重要意义,而且为在治疗开发中靶向 IL-9 反应性肺巨噬细胞提供了理论依据。
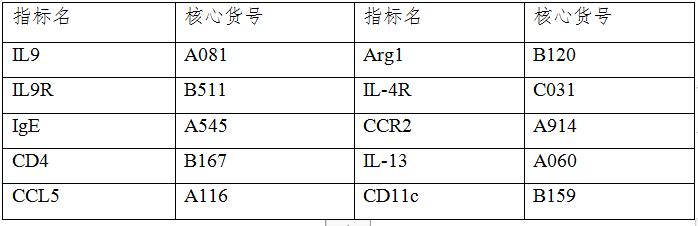
云克隆开发了上述研究中涉及的相关指标的蛋白、抗体、ELISA试剂盒等产品以助力肿瘤治疗相关研究,部分指标节选如下,供参考。